ARSEN
ARSEN (As - latinski - arsenium)
Kemijski element arsen nosi u periodnom sustavu elemenata simbol As, atomski (redni) broj mu je 33
Atomska masa mu iznosi 74,92160(2).
Internacionalni naziv: Arsenum
Oksidacijska stanja: -3, 3, 5
Talište / Vrelište: (K) 1090 (pod tlakom) / 889 (sublimira)
Elektronegativnost: 2,18 / 5,3 eV
Konfiguracija zadnje ljuske: 3d104s24p3
Element je: Polumetal
Spada u grupu: 15 / Va
Spada u skupinu: Dušikova skupina
SVOJSTVA:
ARSEN (As, latinski - arsenium) je kemijski element sa simbolom As i atomskim brojem 33. U periodnom sistemu elemenata svrstan je u 4. periodu i 5. glavnu grupu (grupa 15) odnosno u dušikovu grupu. U prirodi se veoma rijetko može naći samorodan, uglavnom je rasprostranjen u obliku sulfida.
Spada u polumetale, koji ovisi od modifikacije pokazuje metalne ili nemetalne osobine.
Spojevi arsena su poznati od antičkih vremena. Iako je većina spojeva izuzetno otrovna, neki od njih se koriste kao sastavni dijelovi nekih lijekova. Arsen se koristi i za dotiranje poluvodića i kao osnovni dio za III-V poluvodiće kao što je galijarsenid.
ARSEN pripada u mikroelemente i pripada u kategoriju najjačih otrova, naročito njegov anorganski dio. Arsen nam prijeti naročito iz vode, povrća tretiranim pesticidima (čak se pojavio u voćnim sokovima), sredstvima za čišćenje, bojama i lakovima.
ARSEN pripada u tzv. sistemske i akumulativne otrove a tu se krije i najveća opasnost jer nalazi krvi i ureje mogu biti uredni dok se arsen akumulira u jetri, slezeni, bubrezima i koži, gdje postupno pojačava svoje razorno djelovanje.
Arsen se nalazi u dvije alotropske modifikacije: sivi i žuti arsen. Postojaniji je oblik sivi ili metalni arsen. Struktura rešetke metalnog arsena odgovara strukturi rešetke crnog fosfora. Ohlade li se arsenove pare naglo pomoću vrućeg zraka, dobiva se nepostojana modifikacija – žuti arsen.
On se lako otapa u ugljikovu disulfidu (CS2), a iz te se otopine hlađenjem iskritalizira u prozirne, kao vosak mekane, plastične kristale, koji jako lome svjetlost, a molekule mu imaju građu As4. Slabim zagrijevanjem ili utjecajem svjetla prelazi u sivu modifikaciju. Arsen i njegovi spojevi su otrovni i upotrebljavaju se kao insekticidi, kod izrade pesticida i pigmenta za boje.
Arsenovi spojevi su kumulativni otrovi. Zagrijavanjem na zraku, arsen izgara modrikastim plamenom, uz karakterističan miris po češnjaku, a nastaje i bijeli dim arsenova(III) oksida (As2O3). Upotrebljava se u medicini, industriji boja (bojadisalstvu) i za konzerviranje drva i kože.
Arsen je prvi otkrio Albertus Magnus u 1250.
Arsenovodik (AsH) je bezbojan, vrlo otrovan plin, mirisa po češnjaku.
Arsenopirit je arsenov sulfid željeza (FeAsS).
Dobivanje arsena:
Elementarni sivi arsen može se dobiti termičkim razlaganjem arsenopirita bez prisutnosti zraka pri čemu sublimira prema jednadžbi:
4FeAsS(s) -> 4FeS(s) + As4(g)
Žarenjem sulfidnih ruda (npr. bakrovih) koje sadrže arsen na zraku, pored SO2, dobiva se, kao jedan od nusproizvoda, plinoviti As4O6 koji hlađenjem očvrsne i izdvoji se od ostalih sastojaka.
Čvrsti As4O6 reducira se ugljikom pri čemu nastaje plinoviti arsen koji se hladenjem prevodi u čvrsto stanje.
Svojstva i upotreba arsena:
Najstabilnija modifikacija je alfa - arsen, romboedarske strukture. Ima slojevitu mikrostrukturu, metalni sjaj, čeličnosivu boju, mekan je i vrlo krt.
Provodi električnu struju. Pri atmosferskom tlaku sublimira pri temperaturi 613°C (ne tali se), a pri tlaku od 36,4 k Pa što je tlak vlastitih para, tali se pri 817°C. Parama arsena do 800°C odgovara formula As4, a iznad 1700°C formula As2. S vlažnim zrakom reagira već pri sobnoj temperaturi, a zagrijan na zraku gori modrikastim plamenom stvarajući gusti dim AS2O3 mirisa po češnjaku.
Pri sobnoj temperaturi izravno se spaja s fluorom i klorom, a zagrijan i s bromom, jodom te sumporom. Ne spaja se s dušikom, borom, silicijem i ugljikom. Jake oksidativne kiseline, kao što je koncentrirana dušična (zlatotopka), oksidiraju ga u arsenovu kiselinu dok ga razrijeđena dušična kiselina oksidira u arsenastu kiselinu.
Legira se s većinom metala. Drugi alotrop je žuti arsen (beta - arsen) heksagonske strukture koji nastaje naglim hlađenjem arsenovih para. Mekan je poput voska i ne provodi električnu struju. Nestabilan je i pri sobnoj temperaturi djelovanjem svjetlosti, brzo i lako prelazi u sivi arsen.
Amorfni crni arsen dobiva se sublimacijom arsena bez prisutnosti zraka. Nastaje i razgradnjom arsenovodika zagrijavanjem pri čemu se izlučuje u obliku pare stvarajući zrcalni nanos (tzv. "arsensko zrcalo"). Ova se reakcija koristi za dokazivanje malih količina arsena u slučaju sumnje na trovanje (Marshova proba). Zagrijavanjem na 360°C prelazi u stabilni sivi arsen uz razvijanje topline.
Elementarni arsen nema posebne primjene. U malim količinama koristi se kao dodatak bakru i olovu i nekim legurama da im se poveća otpornost, tvrdoća ili sjaj (npr. dodaje se olovu koje se koristi se za proizvodnju sačme do koncentracije 0,3%). Također se koristi u poluvodičkoj tehnologiji kao dopirajuća primjesa kristala germanija i silicija.
Galijev arsenid koristi se u laserima kao laserski medij. Mnogo je važnija primjena spojeva arsena koji se upotrebljavaju u industriji kože i krzna, u staklarskoj i farmaceutskoj industriji, a najviše u poljoprivredi za zaštitu bilja od biljnih štetočina (vidi o spojevima arsena).
POGUBNO DJELOVANJE ARSENA:
- Arsen se veže na hemoglobin i uzrokuje kemolizu
- Rad bubrega je otežan
- Negativno djeluje na probavni sustav, naročito napada i uništava sluznicu
- Arsen djeluje na enzimske procese prilikom stanične oksidacije (smanjenje kisika)
- U stanicama arsen ima toksičan učinak na kromosome gdje blokira mitotičke metafaze
- Djeluje na glatke mišiće, djelujući na krvožilni sustav, uzrokujući krvarenja
- Arsen povećava propusnost kapilara
- Loše djeluje na dišni sustav
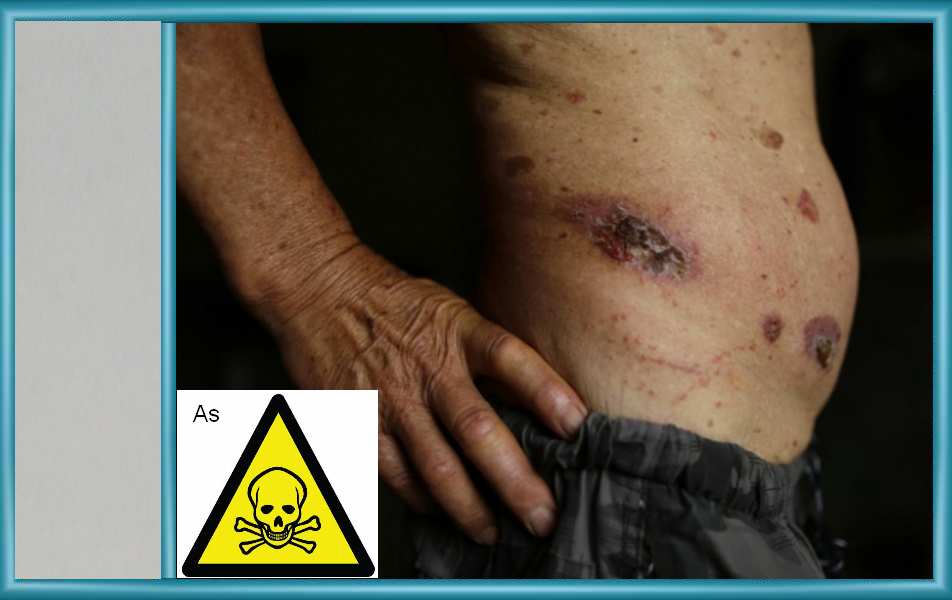
- Arsen stvara velike probleme na koži, preko upala, psorijaze, čireva, sklerodermu i raka kože
- Klinički je ustanovljeno da djeluje na upalu očiju
SIMPTOMI TROVANJA ARSENOM:
- Kronični umor
- Vrtoglavica
- Mučnina
- Povraćanje
- Kašalj, promuklost
- Slabiji rad bubrega
Toksičnost arsena ovisi o obliku u kojem se arsen nalazi. Izrazito toksičan je arsen (III) koji je topljiv u vodi, a teško se izolira, ali lako oksidira pomoću MnO2. Pri trovanju arsenom ljudski organizam prolazi kroz nekoliko stadija; prva faza se manifestira povećanom koncentracijom arsena u krvi, urinu, kosi i noktima, a druga faza pojavom kožnih lezija. U tijelo se arsen može unijeti udisanjem (pojava zapažena u rudnicima u Francuskoj, SAD-u, Švedskoj) i apsorpcijom kroz kožu i širenjem na ostale unutrašnje organe (jetra, bubrezi, pluća itd.). Potpuni mehanizam djelovanja arsena u organizmu još nije poznat. Ovisno o količinama, anorganski arsen unesen u ljudski organizam može imati kronični ili akutni učinak. Akutni učinak podrazumijeva unos većih količina arsena, pri čemu veće doze mogu imati i letalni učinak, dok se kroničnim učinkom smatraju negativne posljedice na ljudsko zdravlje nastale unosom manjih količina arsena kroz duži vremenski period, ono može biti rezultat nakupljanja spojeva arsena u organizmu, kao posljedica konzumiranja vode s povećanom koncentracijom arsena, iako su trovanja zabilježena i pri nižim koncentracijama (oko 2 µgL-1) (Habuda-Stanić i Kuleš, 2002).
Arsen se u praksi iz vode za piće najčešće uklanja slijedećim postupcima: koagulacija i flokulacija, membranski procesi (MF, UF, NF, RO), ionska izmjena i adsorpcijske metode (AWWA, 1999).
Voda za piće:
Voda za piće na području Republike Hrvatske je u većini slučajeva vrlo dobre kvalitete, što dakako nije uobičajeno jer sve češće dolazimo do spoznaje da voda za piće koja nam dolazi iz gradskih vodovoda, bunara, distributivnih mreža ima vrlo veliku koncentraciju kemijskih elemenata ili spojeva. Takva voda s vremenom utječe na naše zdravlje i na zdravlje naših obitelji, te na žalost dovodi do težih zdravstvenih problema. Problematika pojave arsena je upravo takva na području istočne Hrvatske.
S obzirom da su istraživanja ukazala na mogućnost učinkovite primjene aktivnog ugljena u svrhu uklanjanja arsena iz vode za piće, cilj ovog istraživanja bio je ispitivanje učinka i adsorpcijskih karakteristika prirodnog materijala, ljuske lješnjaka, pri vezanju aniona arsena iz modelnih otopina. Učinkovitost uklanjanja arsena adsorpcijom ispitana je ovisno o početnoj koncentraciji arsena, pH-vrijednosti sirove vode, vremenu i temperaturi adsorpcije.
PRIRODNO LIJEČENJE OD DJELOVANJA ARSENA:
SELEN je prirodni element koji ima sposobnost vezanja na arsen, te ga izbaciti iz tijela. Poteškoća je u tome što naša tla imaju sve manje selena. Čak i ako su razine selena u tlu primjerene, sumpor sadržan u umjetnim gnojivima i kiselim kišama koče upijanju selena iz tla. U prirodi selena ima u pivskom kvascu, pšeničnim klicama, preslici, bijelom luku, iznutricama, sjemenu suncokreta.
U našoj zemlji postoji program koji se može nabaviti - MACERAT POLJSKE PRESLICE u ulju od maka, HITOZAN dobiven od oklopa crvenonogih rakova. Inače hitozan je vodeći preparat u čišćenju organizma od otrova i teških metala, tako da vrlo učinkovito upija i odstranjuje arsen iz tijela. Također se može nabaviti KELATNI SELEN u tabletama, koje sadrže 50 µg selena što je dovoljno za jedan dan.
Volite bijelo vino, pivo, prokulice, tunu, losos?
Nedavno provedeno istraživanje pokazalo je da upravo navedene namirnice u ljudskom tijelu povećavaju razine arsena. Tuna i srdela također se nalaze na tom popisu, ali i crno vino, no ipak u znatno manjem omjeru.
Arsen je element koji se prirodno pojavljuje u okolišu, ali nije riječ o zdravom elementu. Dugotrajna izloženost arsenu, čak i malim količinama, povezuje se s povećanim rizikom od raka pluća, kože i mjehura, kao i dijabetesom tipa 2 te kardiovaskularnim bolestima. Ljudi koji jednom tjedno jedu plavu ribu, poput lososa, tune i srdela, imaju sedam posto veće razine arsena u usporedbi s onima koji takvu ribu jedu manje od jednom mjesečno.
Vino i pivo u ovoj priči izgledaju još i gore: ljudi koji su priznali da popiju čašu vina ili dvije i pol čaše piva svaki dan, imaju 20 do 30 puta veće razine arsena u tijelu od onih koji ne piju ova pića. Znanstvenici nisu sigurni koji je razlog ovome. Začuđuje i to što je voda također veliki izvor arsena.
Što se prehrane tiče, znanstvenici tvrde da je najbolji način da izbjegnete izloženost arsenu iz hrane taj da jedete što raznovrsniju hranu i da ne jedete jednake namirnice svaki dan.
Kako je arsen završio u našoj hrani?
Pedesetih godina prošlog stoljeća, arsen se "pod normalno" dodavao drvenini zbog zaštite od insekata, bakterija i gljivica. Nedugo nakon toga, počeo se koristiti i u poljoprivredi kao pesticid. Konvencionalni uzgajivači hrane poveli su se logikom: "Ako funkcionira na drvetu, zašto ne bi i na hrani?". Tako je arsen u "manje toksičnoj formi" na neki način postao dio naše prehrane - a koristi se i danas.
Arsen u najvećoj mjeri kontaminira tlo, tim putem dolazi i u biljke. Nalazimo ga u agrumima, a u najvećoj mjeri kontaminira rižu zbog načina uzgoja u vodenom okruženju. Godine 1955. počeli su primjenjivati arsen čak i kod uzgoja peradi jer osim što ubija bakterija, potiče rast ovih životinja. Zadnjih nekoliko godina zabilježeni su pokušaji zabrane arsena u uzgoju peradi, ali on se i dalje koristi u konvencionalnom načinu uzgoja životinja.
Što možete poduzeti po tom pitanju?
Nažalost, kad se radi o arsenu - organski uzgojena hrana ne znači uvijek sigurnost od ovog toksina. Arsen je svugdje i biljke ga lako apsorbiraju bez obzira na uvjete uzgoja. Zanimljivo je da za arsen čak nije ni standardizirano koje su količine dopustive u hrani. Po tome pitanju svakako treba nešto poduzeti što prije.
Za sad, jedino što možete učiniti je ograničiti unos namirnica koje sadržavaju arsen u većoj mjeri te jesti raznoliku hranu:
- Jesti rižu i njene proizvode jednom do dva puta tjedno
- Ograničiti konzumaciju voćnih sokova od jabuka i agruma